Conception, fonctionnalités et avenir
En biotechnologie industrielle, les fermenteurs à agitation mécanique constituent la base de la culture microbienne à grande échelle. Leur conception influence considérablement l’efficacité du procédé, le rendement du produit et la stabilité opérationnelle globale. Cet article explore les aspects critiques de la conception, de la fonctionnalité et des avancées futures des fermenteurs.
Considérations clés de conception pour les fermenteurs à agitation mécanique
1. Rapport hauteur/diamètre
Le rapport hauteur/diamètre (H/D) d’un fermenteur se situe généralement entre 1,7 et 4, ce qui a un impact direct sur l’efficacité du transfert d’oxygène et les coûts de construction. Des rapports plus élevés améliorent la dissolution de l’oxygène, mais entraînent des coûts structurels et opérationnels plus élevés.
2. Pression de conception
Les fermenteurs standard sont conçus avec une pression nominale de 0,3 MPa, tandis que la pression de fonctionnement reste inférieure à 0,15 MPa pour garantir la stabilité et la sécurité du processus tout au long de la fermentation.
3. Agitateur et structure interne
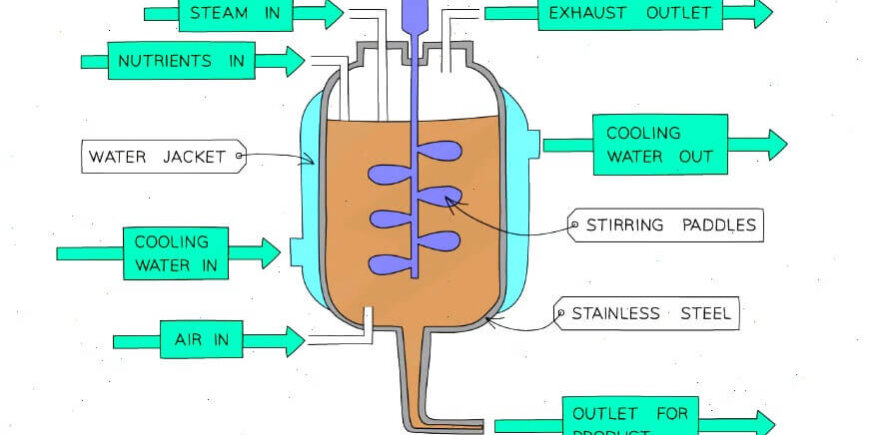
L’agitateur mécanique joue un rôle crucial dans la dissolution de l’oxygène et le mélange du milieu. Une combinaison de plusieurs types d’agitateurs, de chicanes et de serpentins verticaux améliore la turbulence, optimisant ainsi le transfert de masse et de chaleur dans le fermenteur.
4. Performances d’étanchéité
Assurer une étanchéité parfaite est primordial pour prévenir la contamination et les fuites. Des joints mécaniques de haute qualité sur les agitateurs sont essentiels pour maintenir la stérilité du milieu de fermentation.
5. Facilité d’utilisation et de nettoyage
- Les surfaces intérieures polies miroir minimisent l’adhérence du matériau, facilitant ainsi un nettoyage sans couture.
- Les connexions à serrage rapide permettent un démontage, un nettoyage et un entretien faciles.
- Les ports de capteurs intégrés prennent en charge la surveillance et l’automatisation avancées des processus.
6. Efficacité de l’échange thermique
Une zone d’échange thermique adéquate assure des ajustements rapides de la température, empêchant la dégradation des nutriments et maintenant un contrôle précis de la température.
7. Conditions de stérilité
Pour maintenir un processus sans contamination, la stérilité est assurée par :
- Stérilisation des récipients in situ
- Systèmes de filtration d’air stérile
- Maintien de la pression positive
- Mécanismes d’étanchéité à l’air
8. Contrôle des paramètres et automatisation
Les fermenteurs modernes intègrent des systèmes de contrôle automatisés pour réguler les paramètres essentiels du processus, notamment :
- Taux d’aération et niveaux d’oxygène dissous
- Vitesse d’agitation et pression du récipient
- stabilité du pH et de la température
- Stratégies d’alimentation du substrat
- Surveillance de la concentration de la biomasse
- Analyse des gaz d’échappement
9. Systèmes de contrôle intelligents
Les fermenteurs avancés intègrent un contrôle de processus piloté par l’IA, permettant des ajustements en temps réel pour améliorer l’efficacité et la reproductibilité.
10. Personnalisation pour des applications spécifiques
Avec la demande croissante de bioprocédés spécialisés, la conception des fermenteurs évolue vers des solutions sur mesure, adaptées à des souches microbiennes et à des conditions de fermentation spécifiques.
Principe de fonctionnement et optimisation structurelle
Les fermenteurs agités mécaniquement fonctionnent en combinant l’action de cisaillement des pales de l’agitateur avec l’effet de dispersion des distributeurs d’air, améliorant ainsi la solubilité de l’oxygène dans le bouillon de fermentation.
La performance est mesurée à l’aide de :
- Coefficient de transfert d’oxygène (KLa)
- Puissance requise pour le transfert d’oxygène
Optimisation de la sélection des agitateurs pour la culture microbienne
1. Besoins en oxygène
- Les microbes aérobies nécessitent un transfert d’oxygène élevé, ce qui nécessite un mélange air-liquide efficace.
2. Sensibilité au cisaillement
- Certains microbes sont très sensibles aux forces de cisaillement, nécessitant des impulseurs à faible cisaillement tels que des types à palettes ou à hélices.
3. Viscosité du bouillon de fermentation
- Les milieux à haute viscosité nécessitent une agitation puissante, les turbines étant particulièrement efficaces.
4. Dispersion des bulles
- Les conceptions d’agitateurs efficaces facilitent la formation de petites bulles, améliorant ainsi l’efficacité du transfert d’oxygène.
5. Distribution de chaleur
- La dissipation uniforme de la chaleur assure la stabilité de la fermentation et empêche la surchauffe localisée.
6. Suspension solide
- Pour les processus de fermentation impliquant des solides, les agitateurs doivent assurer une suspension uniforme des particules pour éviter la sédimentation.
7. Modèles d’écoulement pour un mélange efficace
- Flux axial : prend en charge le mélange à grande échelle et la circulation des fluides.
- Écoulement radial : améliore la turbulence locale, la dispersion des bulles et la solubilité de l’oxygène.
8. Sélection du matériau de l’agitateur
- Les matériaux doivent être résistants aux produits chimiques, conformes aux normes d’hygiène et de sécurité alimentaire.
9. Taille et configuration de l’agitateur
- La taille et la forme de la turbine doivent être adaptées à la dynamique des fluides et aux besoins de transfert d’oxygène du fermenteur.
10. Systèmes multi-agitateurs
- Les grands fermenteurs peuvent nécessiter plusieurs agitateurs, disposés stratégiquement pour éliminer les zones mortes et assurer un mélange uniforme.
L’avenir de la conception des fermenteurs : automatisation et innovation
À mesure que la biotechnologie progresse, les fermenteurs évoluent vers des systèmes auto-optimisés. L’intégration de capteurs intelligents, d’un contrôle piloté par l’IA et d’une personnalisation modulaire propulse la fermentation industrielle vers plus de précision, d’efficacité et de durabilité.
En adoptant ces avancées technologiques, les systèmes de fermentation modernes sont sur le point de redéfinir le biotraitement et d’accélérer la production microbienne à l’échelle industrielle, jetant ainsi les bases de futures avancées en biotechnologie.